21. Produși de condensare ai monozaharidelor
Cuprins:
21.1. Introducere21.2. Dizaharide
21.3. Polizaharide
21.1. Introducere
Condensarea monozaharidelor pentru a obține oligozaharide sau polizaharide, este un proces biochimic complex cu importanță în lumea vie. Prin simplificare, se poate considera că se rezumă la eliminarea apei între grupele hidroxil, –OH, din două sau mai multe molecule de monozaharide.
21.2. Dizaharide
Dizaharidele se obțin prin eliminarea unei molecule de apă între două molecule de monozaharide identice sau diferite. Eliminarea apei se poate desfășura în două moduri:
- în cazul în care eliminarea apei are loc între hidroxilul glicozidic de la o moleculă de monozaharidă și o grupă hidroxil, în general, din poziția 4, de la cealaltă monozaharidă, legătura eterică formată (C–O–C) se numește legătură monocarbonilică.
În situația în care hidroxilul glicozidic implicat în condensare provine dintr-un anomer β, atunci legătura eterică este β-glicozidică. De exemplu, în celobioză, legătura eterică este monocarbonilică β-glicozidică.
Legăturile eterice β-glicozidice sunt hidrolizate de β-glicozidaze. Reacția de hidroliză a celobiozei este catalizată de emulsină, o β-glicozidază.
- în cazul în care eliminarea apei are loc între grupele hidroxil glicozidice ale celor două monozaharide, legătura eterică (C–O–C) formată se numește legătură dicarbonilică.
Natura legăturii eterice influențează proprietățile dizaharidelor.
Dizaharidele cu legătură monocarbonilică se caracterizează prin:
- au un hidroxil glicozidic liber și astfel pot să treacă în forma carbonilică, dând reacțiile specifice acesteia;
- astfel de dizaharide există sunt forma a 2 anomeri α și β și prezintă mutarotație;
- se oxidează și reduc reactivii Tollens și Fehling;
- sunt dizaharide reducătoare.
Maltoza este un exemplu de dizaharid reducător. La fel și β-celobioza.
Dizaharidele cu legătură dicarbonilică se caracterizează prin:
- nu au hidroxilul glicozidic liber și astfel nu pot trece în forma carbonilică și nu pot da reacțiile specifice acesteia: fenomenul de mutarotație, reducerea soluțiilor Tollens și Fehling;
- sunt dizaharide nereducătoare.
Zaharoza este un exemplu de dizaharid nereducător.
Trehaloza (alcătuită din 2 molecule de α-D-glucopiranoză) este un exemplu de dizaharid nereducător care se întâlnește în ciuperci, drojdii și în unele plante superioare.
Maltoza
Maltoza prezintă următoarele caracteristici:
- se întâlnește în natură în cantități mici în aproape toate plantele;
- în cantități mari se află în cerealele germinate – orz încolțit;
- se mai numește și zahăr de malț, denumire de la extractul apos al orzului încolțit, denumit malț;
- în industrie, se obține prin hidroliza enzimatică a amidonului;
- este un intermediar în fabricarea berii și a alcoolului etilic;
- este hidrolizată de maltaza din drojdia de bere (este o α-glicozidază).
Zaharoza
Zaharoza prezintă următoarele caracteristici:
- formula ei moleculară: C12H22O11;
- este dizaharidul cel mai răspândit în natură;
- se folosește aproape exclusiv în alimentație;
- se întâlnește în trestia de zahăr – 14-20%; sfecla de zahăr – 16-20%;
- din plantele enumerate mai sus se extrage industrial;
- este materie primă pentru produsele zaharoase: bomboane, ciocolată și altele;
- se întâlnește în: morcovi, pepeni galbeni, zmeură, piersici, caise, și multe altele;
- uzual, este denumită zahăr;
- zahărul solid extras din trestia de zahăr este cunoscut indienilor cu 3000 de ani î. Hr.;
- în 1747, chimistul german Margraff a obținut zahărul din sfecla de zahăr;
- este utilizat în alimentație și în industria alimentară;
- prezintă un important aport energetic: 1 g zahăr eliberează prin oxidare biochimică (asimilare) 3,7 - 4,2 kcal sau 17,55 kJ;
- prin hidroliza acidă sau enzimatică a zaharozei se obține un amestec echimolecular de D-glucoză și D-fructoză;
- zaharoza este dextrogiră: [α]D=+66,5°;
- prin hidroliză, soluția este alcătuită din D-glucoză slab dextrogiră și D-fructoză puternic levogiră, deci soluția rezultată este levogiră ([α]D= –22°);
- din acest motiv, amestecul de glucoză și fructoză obținut prin hidroliza zahărului, poartă numele de zahăr invertit și reprezintă mierea artificială;
- zaharoza poate fi hidrolizată de maltază (α-glicozidază) și de invertază (β-glicozidază, enzimă specifică ce va acționa asupra legăturii β-glicozidice din β-D-fructofuranoză).
Proprietățile fizice ale zaharozei:
- este substanță solidă, cristalizată, incoloră;
- este solubilă în apă;
- este greu solubilă în alcool;
- prezintă gust dulce;
- punctul de topire: 185°C.
Proprietăți chimice
ACTIVITATE EXPERIMENTALĂ
Mod de lucru:
1. Într-o capsulă se introduc aproximativ 5 g de zahăr și se încălzește capsula în flacără.
Observații:
1. Prin încălzire, zahărul s-a topit mai întâi și apoi s-a colorat în brun (s-a caramelizat). Prin încălzire ușoară, zaharoza se topește. Prin răcirea zaharozei topite, aceasta se transformă într-o masă amorfă, care prin încălzire la peste 185°C, capătă o culoare brună, se caramelizează și apoi se carbonizează (devine neagră).
Lactoza
Lactoza prezintă următoarele caracteristici:
- este o dizaharidă cu legătură monocarbonilică;
- legătura β-glicozidică este din partea galactozei;
- se întâlnește în lapte în proporție de aproximativ 5%;
- se formează în glanda mamară;
- prin hidroliză rezultă D-glucoză și D-galactoză.
21.3. Polizaharide
Polizaharidele sunt compuși macromoleculari naturali obținuți prin policondensarea biochimică a unor monozaharide. Structura macromoleculei influențează semnificativ proprietățile polizaharidelor.
Amidon
Amidonul se caracterizează prin:
- este un polizaharid format din resturi ale unui izomer al glucozei (diferit de cel din alcătuirea celulozei);
- formula moleculară: (C6H10O5)n;
- este larg răspândit în regnul vegetal;
- este polizaharidul de rezervă al plantelor;
- sub formă de cocă fiartă sau coaptă, amidonul reprezintă hrana de bază a omului;
- se întâlnește în cantitate mare în boabele de orez (62-82%), boabele de porumb (65-72%), semințe (boabe) de grâu (57-75%) și în tuberculii de cartofi (14-20%, poate ajunge și până la 24%);
- din sursele enumerate mai sus poate fi obținut și industrial;
- se formează în părțile verzi ale plantelor, de unde o parte este trecută într-o formă solubilă care are rolul de a hrăni planta, iar altă parte se depune în rădăcinile, tulpinile și semințele plantelor, funcționând ca rezervă de hrană pentru perioadele ulterioare de vegetație;
Amidonul nu este o substanță unitară, acesta se compune din:
- amiloză (10-20%) – partea solubilă, în reacție cu iodul dă o colorație albastră intensă (compuși de incluziune ai iodului în golurile din structura amidonului); în cea mai mare parte reprezintă miezul granulei de amidon; formula generală: H(C6H10O5)nOH, sau mai simplu: –(C6H10O5)n–, unde n = 300 – 1200, în funcție de specia vegetală în care se găsește;
- amilopectină (80-90%) – partea insolubilă, în reacție cu iodul dă o colorație roșie-violetă (slab purpuriu); reprezintă învelișul granulelor de amidon; formula generală similară amilozei: –(C6H10O5)n–, unde n = 6.000 – 36.000;
Amiloza este un polizaharid din alcătuirea amidonului. Amiloza este alcătuită din resturi de α-D-glucopiranoză unite în pozițiile 1-4 prin legături monocarbonilice α-glicozidice. Astfel, moleculele de amiloză nu sunt ramificate. Unghiul format între covalențele C–O din puntea eterică, are valoarea de 111°. Punțile eterice din amiloză prezintă aceeași orientare, adică atomii de oxigen sunt dispuși pe aceeași parte a axei macromoleculei. Din acest motiv, macromoleculele de amiloză sunt răsucite în spirală. Moleculele de iod pot să fie absorbite în canalul de la interior al spiralei, caz în care apare colorația albastră persistentă. Motivul pentru care amiloza este solubilă în apă caldă este dat de structura mai simplă a acestei macromolecule, permițând astfel accesul moleculelor de apă în jurul amilozei.
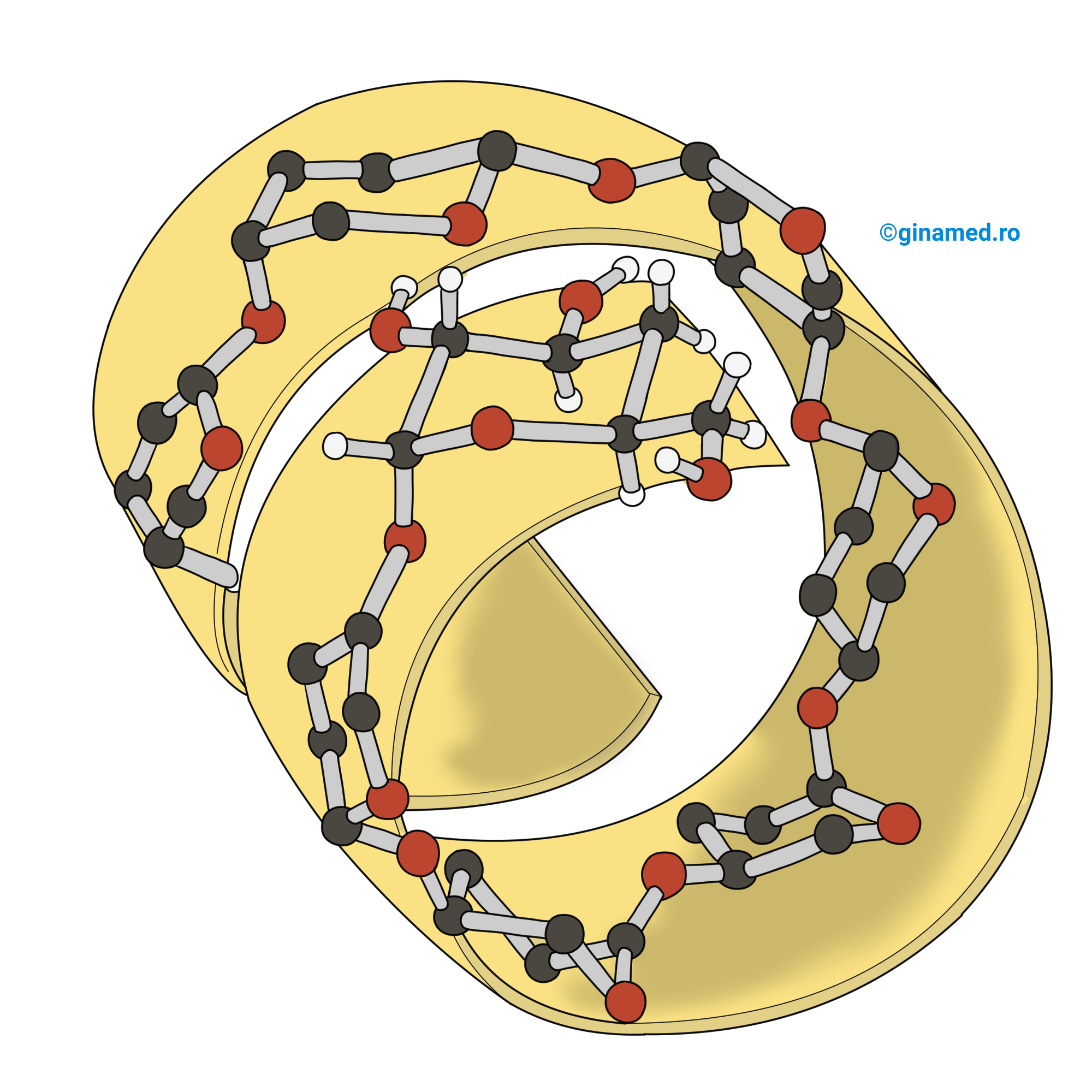
Amilopectina este celălalt polizaharid din alcătuirea amidonului. Amilopectina are o structură ramificată, alcătuită din resturi de α-D-glucopiranoză unite în pozițiile 1-4 și din loc în loc în pozițiile 1-6 prin legături monocarbonilice α-glucozidice. La fel ca și amiloza, și moleculele de amilopectină sunt răsucite în spirală. Datorită formei mai complicate a moleculelor de amilopectină, accesul moleculelor de iod în canalele spiralelor este mai dificil. Amilopectina este insolubilă în apă caldă. În amilopectină, ramificațiile se întâlnesc la intervale de 25 de unități de glucoză și fiecare ramificație este alcătuită din 16-26 unități de glucoză, valoare care depinde de specia vegetală. Catenele laterale se pot ramifica la rândul lor.

Hidroliza amidonului
Hidroliza în mediu acid este, în general, o hidroliză totală și conduce la monozaharidele constituente.
Întreruperea hidrolizei acide sau enzimatice a amidonului, conduce la un sirop format din dextrine, maltoză și glucoză, denumit melasă amidonată sau sirop de porumb. Acesta este folosit pentru a îndulci produsele de cofetărie.
În mediul viu, reacțiile de hidroliză sunt catalizate de enzime specifice. Legăturile eterice α-glicozidice sunt hidrolizate de α-glicozidaze. Maltaza din bere este un exemplu de α-glicozidază care catalizează reacția de hidroliză a maltozei.
Legăturile eterice β-glicozidice sunt hidrolizate de β-glicozidaze. Reacția de hidroliză a celobiozei este catalizată de emulsină, o β-glicozidază, întâlnită în sâmburii de migdale amare. Sau altfel spus, celobioza este hidrolizată de emulsină, o β-glicozidază.
În funcție de natura enzimelor care sunt implicate în hidroliza unor zaharide, se poate identifica configurația hidroxilului glicozidic. În cursul procesului de digestie are loc hidroliza treptată a amidonului până la D-glucoză. Amilaza salivară, enzimă secretată de glandele salivare în cavitatea bucală, scindează amidonul în dextrine (oligozaharide superioare) și eventual până la stadiu de maltoză.
Amilaza salivară își continuă activitatea ei enzimatică până la nivelul stomacului, când aciditatea sucului gastric o inactivează. Amilaza pancreatică este o altă enzimă care intervine în intestin și hidrolizează amidonul la maltoză, trecând intermediar prin stadiul de dextrine. În final, sub acțiunea α-glicozidazei intestinale, maltoza este scindată în D-glucoză. Glucoza se absoarbe la nivelul intestinului subțire și reprezintă principala sursă de energie a organismului. În cazul unui exces de glucoză în organism, acesta este depus la nivelul ficatului și în mușchi, în cantități mai mici. Glicogenul constituie polizaharida de rezervă pentru om și animale. Structura acestuia se aseamănă cu a amilopectinei, însă macromoleculele sunt mai mici și mai ramificate comparativ cu cele ale amilopectinei.
Amidonul din anumite cereale (de exemplu, din malț sau orz încolțit) este folosit ca materie primă în industria berii și a băuturilor alcoolice.
Proprietăți fizice ale amidonului:
- pulbere albă, amorfă;
- fără gust dulce;
- insolubilă în apă rece;
- în apă caldă, la 90°C, granulele de amidon se umflă, după care se sparg și formează soluții vâscoase; la rece, acestea se transformă în gel, denumit cocă sau clei de amidon. Coca este alcătuită numai din amilopectină deoarece este insolubilă în apă caldă.
Utilizări ale amidonului:
- apret, agent de încleiere în industria textilă;
- absorbant, la fabricarea de cașete, aditivi de tablete, pansamente și la prepararea unor pulberi în industria farmaceutică;
- pentru obținerea etanolului;
- sub formă de cocă coaptă sau fiartă în alimentație.
ACTIVITATE EXPERIMENTALĂ
Reacția amidonului cu iodul
Observații: Substanța din compoziția cartofului și făinii dă în reacție cu iodul, o colorație albastru intensă, iar cea din măr rămâne lasă aproape neschimbată culoarea soluției de iod. Explicația este dată de faptul că amidonul din cartof reacționează cu iodul, iar celuloza din măr, nu. Această reacție este utilizată pentru identificarea amidonului în produsele alimentare.
Celuloza
Celuloza se caracterizează prin:
- este un polizaharid format din resturi ale unui izomer spațial al glucozei (β-D-glucopiranoză), unite ca urmare a eliminării apei între două grupe hidroxil, –OH;
- formula moleculară: –(C6H10O5)n–, unde n = 300 – 3400, dependent de specia vegetală din care provine;
- celuloza formează scheletul țesuturilor lemnoase ale plantelor superioare, dar și al ierbii: formează părțile de susținere ale plantelor împreună cu lignina și alți compuși necelulozici, atribuind rezistență mecanică și elasticitate plantelor; astfel, celuloza este cel mai răspândit compus organic de pe Pământ, din punct de vedere cantitativ;
- prezintă structură fibrilară;
- fibrele celulozice sunt fibrele de bumbac;
- industrial, celuloza se obține din lemn în stare pură, stuf și paie, plante cu conținut bogat în celuloză;
- organismul uman nu deține enzime pentru hidroliza celulozei, astfel, aceasta nu constituie o substanță nutritivă pentru om.
Conținutul procentual (%) în celuloză în diferite plante:
| Plante | Celuloză |
|---|---|
| foioase | 40-50% |
| conifere | 45-50% |
| ierburi | 25-40% |
| bumbac, in, cânepă | 80-95% |
Atomii de oxigen din punțile eterice din celuloză, sunt orientați alternativ de o parte și de alta a axei macromoleculei și astfel, macromoleculele de celuloză prezintă o orientare liniară. Structura lor filiformă permite orientarea lor paralelă și realizarea unui număr mare de legături de hidrogen între grupele hidroxil din macromoleculele învecinate. Astfel, macromoleculele sunt foarte strâns împachetate, iar firul de celuloză este rezistent. Moleculele de apă nu pot să pătrundă printre macromoleculele de celuloză și astfel se justifică insolubilitatea lor în apă.
Faptul că grupele hidroxil din celuloză sunt implicate în legături de hidrogen, le face să fie mai puțin reactive. Cu toate acestea, celuloza formează esteri ai acizilor anorganici și organici cu utilizări importante.
Proprietăți fizice ale celulozei:
- substanță solidă, albă;
- inodoră, insipidă;
- slab higroscopică;
- insolubilă în apă și în cea mai mare parte a solvenților.
Proprietăți chimice
Prin încălzire, celuloza se carbonizează fără a se topi.
ACTIVITATE EXPERIMENTALĂ
Dizolvarea celulozei
Sunt necesare două eprubete pentru a observa dizolvarea celulozei. În prima se aduc 5 mL de apă, iar în cea de-a doua se aduc 5 mL de reactiv Schweitzer. În fiecare din cele două eprubete se aduc bucățele de hârtie sau de vată.
Observații: Hârtia sau vata sunt insolubile în apă, însă se dizolvă în reactivul Schweitzer.
În fiecare unitate de glucoză din celuloză, pot să fie esterificate una, două sau trei grupe hidroxil. Dependent de gradul de esterificare, produșii rezultați prezintă variate utilizări:
- fulmicotonul (nitrat de celuloză care conține aproximativ 12-13% azot), se folosește la obținerea pulberii fără fum în industria explozivilor;
- esteri ai celulozei cu un conținut mai redus în azot (aproximativ 10-11%) sunt utilizați pentru fabricarea lânii de colodiu (de aceea se mai numesc, colodiu), din care se obține celuloidul.
Celuloidul constituie o masă transparentă obținută din colodiu și camfor. Acesta a fost folosit cu rol de suport pentru filmele fotografice și cinematografice. Datorită proprietăților sale ușor inflamabile, celuloidul a fost înlocuit cu acetat de celuloză, mai puțin inflamabil.
- nitrații de celuloză cu conținut scăzut în azot sunt folosiți pentru fabricarea nitrolacurilor și nitroemailurilor (lacuri de acoperire cu uscare rapidă și luciu puternic).
Tratarea celulozei cu amestec de anhidridă acetică și acid acetic
Acetații de celuloză sunt folosiți pentru fabricarea de fibre, folii, filme de siguranță, lacuri, la fabricarea mătăsii acetat, filme cinematografice și a unor materiale plastice care se aseamănă cu celuloidul, denumite celon.
Acetații de celuloză se dizolvă în acetonă. Soluția rezultată se filtrează la cald, când acetona se evaporă și se recuperează, iar firul de acetat de celuloză coagulează și se întărește. Țesăturile de mătase acetat sunt mai rezistente, însă mai puțin higroscopice comparativ cu cele din vâscoză.
Tratarea celulozei cu hidroxid de sodiu și sulfură de carbon
Hidroliza celulozei
Animalele superioare nu dețin în tubul digestiv enzima care hidrolizează celuloza, denumită celulază. Din acest motiv, aceste animale nu pot să valorifice celuloza pentru hrană. Pe de altă parte, melcii, omizile, viermii și numeroase microorganisme secretă celulază și enzime care hidrolizează celobioza, permițându-le astfel să se hrănească cu celuloză. Astfel, cantități mari de celuloză din plantele moarte sunt procesate (transformate) de către bacterii în materiale cu valoare nutritivă pentru sol și în dioxid de carbon în cadrul proceselor de putrezire. În acest fel se asigură echilibrul ecologic.
Utilizări ale celulozei:
- obținerea hârtiei – principala utilizare;
- pentru obținerea mătăsii artificiale (de tip vâscoză și acetat);
- pentru obținerea unor materiale pentru bandaj – vată;
- la obținerea unor materiale explozive;
- la obținerea altor derivați ai celulozei.
Bibliografie:
- Chimie - manual pentru clasa a X-a; Autori: Luminița Vlădescu, Corneliu Tărăbășanu - Mihăilă, Luminița Irinel Doicin. Grup Editorial ART, București, 2005
- Chimie C1 - manual pentru clasa a XI-a; Autori: Elena Alexandrescu, Viorica Zaharia, Mariana Nedelcu. Editura LVS Crepuscul, colecția Educațional, Ploiești, 2006

